2. 湖南农业大学动物医学院, 长沙, 410128
 作者
作者  通讯作者
通讯作者
水生生物研究, 2012 年, 第 1 卷, 第 2 篇 doi: 10.5376/aor.cn.2012.01.0002
收稿日期: 2012年04月15日 接受日期: 2012年06月12日 发表日期: 2012年06月21日
建议最佳引用格式:
引用格式(中文):
孙科军等, 2012, 斑鳜myostatin基因及其启动子的克隆与序列分析, 水生生物研究Vol.2 No.2 pp.7-13 (doi: 10.5376/aor.cn.2012.01.0002)
引用格式(英文):
Sun et al., 2012, Cloning and Sequence Analysis of the Myostatin Gene and its Promoter in Golden Mandarin Fish (Siniperca scherzeri), Shuisheng Shengwu Yanjiu (Aquatic Organism Research) Vol.1 No.2 pp.7-13 (doi: 10.5376/aor.cn.2012.01.0002)
采用Tail-PCR和常规PCR技术首次克隆出斑鳜myostatin基因及其启动子序列。经生物信息学分析发现,斑鳜myostatin基因由3个外显子和2个内含子组成,编码区1 131 bp,共编码376个氨基酸。斑鳜myostatin启动子区域大小为840 bp,存在1个TATAA-box、4个E-box和1个CAAT-box作用元件。利用软件CLUSTALW和MEGA3.1构建14种硬骨鱼的myostatin启动子的系统进化树结果表明:斑鳜同大口黑鲈亲缘关系最近,与鲤鱼和缨野鲮亲缘关系较远,其结果与传统形态学分类中的亲缘关系一致。斑鳜myostatin基因及其启动子克隆与特征分析,将为进一步研究鱼类myostatin基因的表达调控及其功能分析提供参考。
肌肉生长抑制素(myostatin, MSTN)基因是McPherron和Lee (1997)在研究TGF-β (transforming growth factor-β)家族时,用该家族基因保守序列设计简并性引物对小鼠cDNA文库进行扩增得到的一个新基因。编码376个氨基酸,具有TGF-β超家族的典型结构,但与其它TGF-β家族成员的同源性很低,因而被归为新一类:GDF-8 (Mcpherron et al., 1997)。Myostatin基因主要在动物骨骼肌中特异性表达并对肌肉的生长发育起到负调控作用(Rios et al., 2004)。超量表达可以导致动物肌肉萎缩,而其突变则使动物产生双肌现象(Mcpherron et al., 1997;Schuelke et al., 2004)。实验发现,将重组人myostatin蛋白载体肌注于裸鼠后腿,可导致肌肉和脂肪显著减少(Zimmers et al., 2002)。而敲除myostatin基因的小鼠肌肉质量会显著增加(Welle et al., 2007)。而定向敲除myostatin基因可明显抑制由糖皮质激素诱发的肌肉萎缩(Gonzalez-Cadavid et al., 1998)。由近来的研究可知,与myostatin 基因编码区相比,myostatin基因的启动子区域序列不同物种间差异较高,意味着myostatin基因的转录调控模式在不同物种间可能存在着差异(Gu et al., 2004; Du et al., 2005;Yu et al., 2005)。有少数研究对人、鼠和牛等myostatin 基因启动子进行了探讨,发现一些转录因子(如MyoD, Smad, FoxO和MEF-2)对myostatin基因的转录和表达起到调控作用(Ma et al., 2001; Spiller et al., 2002; Crisa et al., 2003; Salerno et al., 2004; Forbes et al., 2006; Allen and Unterman, 2007),然而,这方面仍有许多未知领域有待进一步研究。
目前已有较多鱼类的myostatin的研究,比如:采用RNAi途径,给斑马鱼(Danio rerio)受精卵注射myostatin 的C末端dsRNA,导致斑马鱼早期胚胎的增生或肥大(Acosta et al., 2005);斑点叉尾鲴(Ictalurus punctatus)经外源糖皮质激素处理12 h后,myostatin的表达下降(Rodgers et al., 2003);虹鳟(Oncorhynchus mykiss) myostatin前体蛋白在生长激素处理后升高(Weber et al., 2005);转GH (生长激素)基因大麻哈鱼(Salmo salar)白肌组织也具有较高的myostatin前体水平等(Biga et al., 2004)。Myostatin作为一种肌肉生长的负性调控因子,通过对该基因进行遗传改造,在渔业方面有着广阔的商业前景。斑鳜俗称花桂或黑桂,隶属于鲈形目(Perciformes)、鳜亚科(Sinipercinae)、鳜属(Siniperca),是我国著名的淡水经济鱼类,其肉质鲜美,口感细腻,富含不饱和脂肪酸,有“淡水石斑”之称(符贵红等, 2008)。与翘嘴鳜和大眼鳜等常见的鳜鱼养殖品种相比,斑鳜虽生长周期较长,但其粗蛋白含量高,脂肪和灰分较低,整体营养价值和肉质品质较高,且疾病少、抗病能力强,具有较大的经济价值和应用前景(苏胜齐等, 2005)。本研究通过对斑鳜myostatin启动子,编码区和非编区的克隆及其结构特征的初步分析,为进一步研究斑鳜肌肉生长和发育调控奠定基础。
1结果与分析
1.1斑鳜myostatin结构基因和启动子序列片段PCR扩增
以斑鳜白肌基因组DNA为模板,分别经三轮Tail-PCR和两组常规PCR反应来克隆myostatin的启动子和myostatin的结构基因片段。PCR产物经的1%琼脂凝胶电泳检测,最终得到的一个约1 kb大小的上游调控序列及两条分别约为2 kb和1 kb的结构基因片段(图1)。
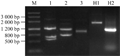 图1斑鳜myostatin基因和启动子PCR产物的琼脂糖凝胶电泳 |
1.2 PCR产物测序
将PCR产物纯化回收,测序,然后将3个片段的测序结果进行拼接,得到一个3 228 bp的片段,其中上游调控序列长868 bp,结构基因长2 360 bp,结构基因由3个外显子和2个内含子组成,外显子大小依次为379 bp、371 bp和381 bp;内含子大小分别为395 bp和830 bp。外显子总长为1 131 bp,共编码376个氨基酸(图2)。氨基酸序列分析表明,编码的氨基酸分子量大小为42.55 kD,等电点pI为5.55,氨基酸整体偏酸性。
 图2斑鳜肌肉生长抑制素结构基因及上游调控序列分析 |
1.3启动子序列系统进化分析
从Genebank中查询得到大口黑鲈、斑马鱼、虹鳟鱼、大黄鱼、花鲈、黄鳍棘鲷、鲤鱼、缨野鲮、尖吻鲈、尼罗尖吻鲈、大鳞大麻哈鱼、金头鲷、比氏骨鳊共13种鱼的myostatin的启动子序列,通过与本实验克隆出来的斑鳜myostatin启动子进行比对。然后利用CLUSTALW和MEGA3.1软件N-J法构件系统发育树(图3),bootstrap自举值取1 000次,显示不同种属鱼类的进化及亲缘关系。
由图3表明:斑鳜、大口黑鲈、大黄鱼、花鲈、黄鳍棘鲷、尖吻鲈、尼罗尖吻鲈、金头鲷、比氏骨鳊这几种鲈形目鲈亚目鱼类在一个大的分支上,斑鳜与大口黑鲈的亲缘性最近;属于鲤形目鲤科的鲤鱼、缨野鲮、比氏骨鳊以及属于鲑形目鲑科的虹鳟鱼、大鳞大麻哈鱼分别在另两个大的分支上。图中myostatin启动子进化树所表明的鱼类亲缘关系及其本身的分类地位,与传统形态学分类结果相一致。
.png) 图3 14种鱼类myostatin启动子序列的NJ系统进化树 |
2讨论
Tail-PCR是一种用来克隆已知序列两端的未知序列的新方法,特异性高,重复性好,能快速获得目标片段。避免了基因组步行法对高质量基因组DNA的要求,与普通PCR一样,可以使用低质量的基因组DNA做模板。本试验利用Tail-PCR的方法克隆出斑鳜myostatin的上游调控序列,长度约为860 bp。PLACE预测结果显示,该基因上游调控区除含有一个核心启动序列(732~781 bp)外,还有I-box (156~160 bp)、TATAA box (730~744 bp)、CAAT-box (698~701 bp)及4个E-box (26~31 bp, 287~292 bp, 589~594 bp, 608~613 bp)等启动子特征性调控元件的存在。进一步分析表明:斑鳜E-box3是MyoD转录因子结合位点,MyoD可通过与E-box结合调控其下游靶基因myostatin的转录和表达,对肌肉的生长发育有着重要的调控作用(Langley et al., 2002; Østbye et al., 2007)。作为MyoD家族转录因子结合位点的E-box元件同样在斑马鱼(Xu et al., 2003)、石斑鱼(Chen et al., 2007)、虹鳟(Garikipati et al., 2006)、花鲈(Ye et al., 2007)、大西洋鲑(Østbye et al., 2007)等硬骨鱼的myostatin启动子序列中被发现。调控序列中的CAAT-box元件可极大提高基本启动子的转录效率(孙晓红等, 2002),对myostatin基因的转录水平也有着较大的影响。
对myostatin启动子的进化分析表明:斑鳜myostatin启动子与其它13种鱼亲缘关系的远近和本身的分类学地位,与传统形态学分类结果相一致。由此我们可以假设,启动子的变化与物种的进化有着相关性,启动子通过碱基变化来改变结构基因的转录水平从而促使物种向着与启动子作用相关的方向进化。
DNA序列分析表明,克隆得到的斑鳜myostatin 结构基因长2 360 bp,由3个外显子和2个内含子组成,外显子大小依次为379 bp、371 bp和381 bp;内含子I和内含子II大小分别为395 bp和830 bp。两个内含子都以GT开始、AG结尾,符合内含子的GT-AG剪接规则。进一步分析发现:内含子I序列中有2个CAAT-box,内含子II序列中有1个TATAA-box,5个CAAT-box等类似启动子调控元件,推测斑鳜myostatin基因内含子可能具有增强该基因转录的功能。同样,典型的调控元件CArG和TATAA-box序列也分别在鲮β-actin基因内含子1和准噶尔雅罗鱼β-actin 基因的第1个内含子中被发现,预示着这些内含子可能作为相应基因启动子的一部分在起始转录表达中有着重要作用(张殿昌等, 2007; 胡文革等, 2010)。
斑鳜myostatin基因推导的氨基酸序列显示:该蛋白在22~23位氨基酸之间存在一个信号肽切割位点,264~267位氨基酸处有RARR (与RXXR相一致)蛋白酶解的加工位点。与其它TGF-β超家族成员蛋白一样,myostatin蛋白以前体形式存在,切除信号肽后,在RXXR位点经蛋白酶水解加工,形成N端编码前肽和C端生物活性区(Lee and McPherron, 2001)。斑鳜myostatin氨基酸序列C端生物活性区的保守性很高,其中有9个异常保守的半胱氨酸,它们以二硫键形式连接形成的“cysteine knot”结构可能与myostatin蛋白及其它TGF-β超家族成员共有的蛋白稳定性及高导热性直接相关(Muller et al., 2002; Barth et al., 2003)。
与哺乳动物相比,虹鳟鱼、大西洋鲑鱼、罗非鱼和石鮨鱼等硬骨鱼类的myostatin基因有两种类型(即myostatin-I和myostatin-II) (Østbye et al., 2001; Rodgers et al., 2003; Garikipati et al., 2007)。本实验克隆的myostatin基因与这些鱼类的myostatin-I 同源性较高,而斑鳜中是否有第二种myostatin基因类型的存在还有待进一步研究。许多研究表明:myostatin基因是哺乳动物肌肉发育中重要的负性调控因子,仅在骨骼肌中特异性表达;而鱼类的myostatin基因在除骨骼肌外的多种组织(如: 脑, 心, 肾, 眼, 肠等)中广泛表达,因此,可推测鱼类myostatin基因的作用可能不仅仅局限于抑制其肌肉的生长发育,还可对鱼类神经系统的发育等多方面产生广泛影响(Garikipati et al., 2007)。本研究对斑鳜myostatin基因及启动子进行了克隆及初步的生物信息学分析,为进一步研究斑鳜myostatin基因的功能及其启动子的调节机制提供了有益的参考。
3材料与方法
3.1试验材料和试剂
鲜活斑鳜(Siniperca scherzeri)购于长沙西长街特种水产品市场,解剖获取鱼背部肌肉,提取基因组DNA用于myostatin的克隆。
OMEGA Mini Plasmid Kit、Gel Extraction Kit、TaKaRa TaqTM PCR试剂盒(购自宝生物有限公司);DNA mark、PMD18-T载体、top10感受态细胞(购自天根生化科技有限公司)。
3.2白肌基因组DNA的提取
称取0.2 g斑鳜的白肌,尽量剪碎,加入1 mL裂解液(10 mmol/L Tris-HCl, pH 8.0; 100 mmol/ L EDTA; 400 mmol/L NaCl; 1% SDS)于玻璃匀浆器中研磨均匀。吸取500 μL匀浆液,加入半粒黄豆大的蛋白酶K,摇匀,56℃消化2~3 h。裂解物分别用等体积的饱和酚、酚/氯仿/异戊醇(25:24:1)和氯仿/异戊醇(24:1)各抽提1次,12 000 r/min离心10 min,取上清液。加1/10体积3 mol/L NaAc和两倍体积的无水乙醇,-20℃沉淀30 min,12 000 r/min,离心10 min,弃上清。70%乙醇漂洗两次,离心,弃废液,干燥。最后用100 μL无菌去离子水溶解。
3.3引物设计和合成
根据Genbank中与斑鳜亲缘性较近物种的myostatin基因序列的比较,设计简并引物AD1和特异性引物Sp1、Sp2及Sp3扩增斑鳜myostatin的启动子。引物F1和R1,F2和R2用于扩增MSTN基因的部分序列,再拼接成一个长片段。所用的引物(表1)均由博尚生物公司合成。
表1引物序列及退火温度 |
3.4 Myostatin基因和启动子的克隆
AD1为14 bp的简并引物,以斑鳜白肌基因组DNA为模板与下游引物SP1进行第一轮扩增,然后以1 μL第一轮产物为模板与下游引物SP2进行第二轮扩增,最后以1 μL第二轮产物继续与下游引物SP3进行第三轮扩增,得到第三轮产物(PCR程序如表2)。以斑鳜基因组DNA为模板,F1和R1为引物进行扩增,程序为94℃ 3 min;94℃ 30 s,56℃ 1 min,72℃ 2 min,36个循环;72℃ 8 min。以F2和R2为引物,斑鳜基因组DNA为模板进行PCR扩增,程序为 94℃ 3 min;94℃ 30 s,58℃ 1 min,72℃ 1 min,36个循环;72℃ 8 min。
.png) 表2 Tail-PCR反应程序 |
3.5 PCR产物的回收和测序
以上PCR产物经1%的琼脂胶电泳分离,切下目的条带,用OMEGA Gel Extraction Kit试剂盒回收。纯化产物连接至PGM-18T载体,转化到top10感受态细胞中,菌落PCR筛选阳性克隆,提取质粒,送博尚生物公司测序。
3.6序列的生物信息学分析
利用DNAMAN软件进行核苷酸及氨基酸序列分析,由PLACE (http://www.dna.affrc.go.jp/PLACE /signalscan.html)预测启动子调控元件及转录起始位点。Splign (http://www.ncbi.nlm.nih.gov/sutils/splign/splign.cgi)进行内含子分析。
作者贡献
孙科军是本研究的试验执行者,完成了采样、基因克隆、数据分析以及论文初稿的撰写与修改;刘希良、王开卓和陈敦学参与了试验的采样和数据分析工作;陈韬和张建社为本研究立意指导;成嘉和褚武英参与本研究的实验设计、论文修改。
致谢
感谢孙志良教授的精心指导和大力支持。
参考文献
Acosta J., Carpio Y., Borroto I., Gonzalez O., and Estrada M.P., 2005, Myostatin gene silenced by RNAi show a zebrafish giant phenotype, J. Biotechnol., 199119(4): 324-331
http://dx.doi.org/10.1016/j.jbiotec.2005.04.023 PMid:16005092
Allen D.L., and Unterman T.G., 2007, Regulation of myostatin expression and myoblast by FoxO and SMAD transcription factors, Am. J. Physiol. Cell Physiol., 292(1): C188-C199
http://dx.doi.org/10.1152/ajpcell.00542.2005 PMid:16885393
Barth D., Kyrieleis O., Frank S., Renner C., and Moroder L., 2003, The role of cysteine knots in collagen folding and stability, partII. Conformational properties of (Pro-Hyp-Gly) model trimers with N-and C-terminal collagen typeIII cysteine knots, Chemistry, 9(15): 3703-3714
http://dx.doi.org/10.1002/chem.200304918 PMid:12898697
Biga P.R., Schelling G.T., Hardy R.W., Cain K.D., Overturf K., and Ott T.L., 2004, Growth hormone differentially regulates muscle myostatin-l and-2 and increases circulating cortisol in rainbow trout (Oncorhynchus mykiss), Gen. Comp. Endocnn., 135(3) 324-333
http://dx.doi.org/10.1016/j.ygcen.2003.10.014 PMid:14723884
Chen Y.M., Wei C.Y., Chien C.H., Chang H.W., Huang S.I., Yang H.L., and Chen T.Y., 2007, Myostatin gene organization and nodavirus-influenced expression in orange-spotted grouper (Epinephelus coioides), Comp. Biochem. Physiol., Part D, 2(3): 215-227
Crisa A., Marchitelli C., Savarese M.C., and Valentini A., 2003, Sequence analysis of myostatin promoter in cattle, Cytogenet Genome Res., 102(1-4): 48-52
http://dx.doi.org/10.1159/000075724
Du R., Chen Y.F., An X.R., Yang XY., Ma Y., Zhang L., Yuan X.L., Chen L.M., and Qin J., 2005, Cloning and sequence analysis of myostatin promoter in sheep, DNA Seq., 16(6): 412-417
http://dx.doi.org/10.1080/10425170500226474 PMid:16287620
Forbes D., Jackman M., Bishop A., Thomas M., Kambadur R., and Sharma M., 2006, Myostatin auto-regulates its expression by feedback loop through Smad7 dependent mechanism, J. Cell Physiol., 206(1): 264-272
http://dx.doi.org/10.1002/jcp.20477 PMid:16110474
Fu G.H., Chu W.Y., Cheng J., Liu F., Liu Z., and Zhang J.S., 2008, Analysis on nutritional components in muscle of Siniperca kneri and Siniperca scherzri, Anhui Nongye Kexue (Journal of Anhui Agricultural Sciences), 36(34): 10522-10523, 15026 (符贵红, 褚武英, 成嘉, 刘芳, 刘臻, 张建社, 2008, 大眼鳜和斑鳜肌肉营养成分分析, 安徽农业科学, 36(34): 10522-10523, 15026)
Garikipati D.K., Gahr S.A., and Rodgers B.D., 2006, Identification, characterization, and quanitative expression analysis of rainbow trout Myostatin-1a and myostatin-1b genes, Journal of Endocrinology, 190(3): 879- 888
http://dx.doi.org/10.1677/joe.1.06866 PMid:17003288
Garikipati D.K., Gahr S.A., Roalson E.H., and Rodgers B.D., 2007, Characterization of rainbow trout myostatin-2 genes (rtMSTN-2a and -2b): Genomic organization, differential expression, and pseudogenization , Endocrinology, 148(5): 2106-2115
http://dx.doi.org/10.1210/en.2006-1299 PMid:17289851
Gonzalez-Cadavid N.F., Taylor W.E., Yarasheski K., Sinha-Hikim I., Ma K., Ezzat S., Shen K.Q., Lalani R., Asa S., Mamitam M., Nair G., Arver S., and Bhasin S., 1998, Organization of the human myostatin gene and expression inhealthy men and HIV-infected men with muscle wasting, Proc. Natl. Acad. Sci., USA, 95(25): 14938-14943
http://dx.doi.org/10.1073/pnas.95.25.14938
Gu Z., Zhang Y., Shi P., Zhang Y.P., Zhu D., and Li H., 2004, Comparison of avian myostatin genes, Anim. Genet., 35(6): 470-472
Hu W.G., Chen C.F., Wang Y.Z., Hao F.X., Cao X.D., and Sheng J.L., 2010, Cloning and sequence analysis of the β- actin gene promoter region of Leuciscus merzbacheri, Dongwuxue Zazhi (Chinese Journal of Zoology), 45(1): 18-26 (胡文革, 陈创夫, 王远志, 郝凤霞, 曹旭东, 盛金良, 2010, 准噶尔雅罗鱼β-肌动蛋白基因启动子克隆及序列分析, 动物学杂志, 45(1): 18-26)
http://dx.doi.org/10.1111/j.1365-2052.2004.01194.x PMid:15566475
Langley B., Thomas M., Bishop A., Sharma M., Gilmour S., and Kambadur R., 2002, Myostatin inhibits myoblast differentiation by down- regulating MyoD expression, J. Biol. Chem., 277: 49831-49840
http://dx.doi.org/10.1074/jbc.M204291200 PMid:12244043
Lee S.J., and McPherron A.C., 2001, Regulation of myostatin activity and muscle growth, Proc. Natl. Acad. Sci., 98(16): 9306-9311
http://dx.doi.org/10.1073/pnas.151270098 PMid:11459935 PMCid:55416
Ma K., Mallidis C., Artaza J., Taylor W., Gonzalez-Cadawid N., and Bbasin S., 2001, Characterization of 5'-regulatory region of human myostatin gene regulation by dexamethasone in vitro, Am J Physiol Endocrinol Metab, 281(6): E1128-E1136 PMid:11701425
Mcpherron A.C., Lawler A.M., and Lee S.J., 1997, Regulation of skeletal muscle mass in mice by a new TGF-β superfamily member, Nature, 387(6628): 83-90
http://dx.doi.org/10.1038/387083a0 PMid:9139826
McPherron A.C., and Lee S.J., 1997, Double muscling in cattle due to mutations in the myostatin gene, Proc. Natl. Acad. Sci., USA, 94(23): 12457-12461
http://dx.doi.org/10.1073/pnas.94.23.12457
Muller Y.A., Heiring C., Misselwitz R., Welfle K., and Welfle H., 2002, The cystine knot promotes folding and not thermodynamic stability in vascular endothelial growth factor, J. Biol. Chem., 277(45): 43410-43416
http://dx.doi.org/10.1074/jbc.M206438200 PMid:12207021
Østbye T.K., Galloway T.F., Nielsen C., Gabestad I., Bardal T., and Andersen Ø., 2001, The two myostatin genes of Atlantic salmon (Salmo salar) are expressed in a variety of tissues, Eur. J. Biochem., 268 (20): 5249-5257
http://dx.doi.org/10.1046/j.0014-2956.2001.02456.x
Østbye T.K., Wetten O.F., Tooming-Klunderud A., Jakobsen K.S., Yafe A., Etzioni S., Moen T., and Andersen Ø., 2007, Myostatin (MSTN) gene duplication in Atlantic salmon (Salmo salar): evidence for different selective pressure on teleost myostatin-1 and-2, Gene, 403(1-2): 159-169
http://dx.doi.org/10.1016/j.gene.2007.08.008 PMid:17890020
Ríos R., Fernández-Nocelos S., Carneiro I., Arace V.M., and Deversa J., 2004, Differential response to exogenous and endogenous myostatin in myoblasts suggests myostatin acts as an autocrine factor in vivo, Endocrinology, 145(6): 2795-2803
http://dx.doi.org/10.1210/en.2003-1166 PMid:14976141
Rodgers B.D., Weber G.M., Kelley K.M., and Levine M.A., 2003, Prolonged fasting and cortisol reduce myostatin mRNA levels in tilapia larvae; short-term fasting elevates, Am. J. Physiol. Regul. Integr. Comp. Physio1., 284(5): R1277-R1286
Salerno M.S., Thomas M., Forbes D., Watson T., Kambadur R., and Sharma M., 2004, Molecular analysis of fiber type-specific expression of murine myostatin promoter, Am. J. Physiol. Cell Physiol., 287(4): C1031-1040
http://dx.doi.org/10.1152/ajpcell.00492.2003 PMid:15189813
Schuelke M., Wagner K.R., Stolz L.E., Hübner C., Riebel T., Kömen W., Braun T., Tobin J.F., and Lee J., 2004, Myostatin mutation associated with gross muscle hypertrophy in a child, N. Engl. J. Med., 350(26): 2682-2688
http://dx.doi.org/10.1056/NEJMoa040933 PMid:15215484
Spiller M.P., Kambadur R., Jeanplong F., Thomas M., Martyn J.K., Bass J.J., and Sharma M., 2002, The myostatin gene is a downstream target gene of basic helix-loop-helix transcription factor MyoD, Mol. Cell Biol., 22(20): 7066-7082
http://dx.doi.org/10.1128/MCB.22.20.7066-7082.2002 PMid:12242286 PMCid:139803
Su S.Q., Zhang H.Q., He Z.Y, and Zhang Z.X., 2005, A comparative study of the nutrients and amno acid composition of the muscle of Siniperca chuatsi and S. Scherzeri, Xinan Nongye Daxue Xuebao (Zirankexue Ban) (Journal of Southwest Agricultural University (Natural Science)), (6): 898-901 (苏胜齐, 张海琪, 何中央, 张祖兴, 2005, 翘嘴鳜和斑鳜肌肉营养成分及氨基酸组成比较, 西南农业大学学报(自然科学版), (6): 898-901)
Sun X.H., Li M.J., and Pan Y.J., 2002, A brief account of promoter cloning, Shijun Xuebao (Acta Edulis Fungi), 9(3): 57-62 (孙晓红, 李明杰, 潘迎捷, 2002, 启动子克隆概述, 食菌学报, 9(3): 57-62)
Weber T.E., Small B.C., and Bosworth B.G., 2005, Lipopolysaccharide regulates myostatin and MyoD independently of an increase in plasma cortisol in channel catfish (Ictalurus punctatus), Domestic Animal Endocrinology, 28(1): 64-73
http://dx.doi.org/10.1016/j.domaniend.2004.05.005 PMid:15620807
Welle S., Bhatt K., Pinkert C.A., Tawil R., and Thornton C.A., 2007, Muscle growth after Post-developmental myostatin gene knockout, Am. J. Physiol. Endocrinol. Metab., 292(4): E985-E91
http://dx.doi.org/10.1152/ajpendo.00531.2006 PMid:17148752
Xu C., Wu G., Zohar Y., and Du S.J., 2003, Analysis of myostatin gene structure, expression and function in zebrafish, J. ExP. Biol., 206: 4067-4079
http://dx.doi.org/10.1242/jeb.00635 PMid:14555747
Ye H.Q., Chen S.L., Sha Z.X., and Liu Y., 2007, Molecular cloning and expression analysis of the myostatin gene in sea perch (Lateolabrax japonicus), Mar. Biotechnol. (NY), 9(2): 262-272
http://dx.doi.org/10.1007/s10126-006-6093-6 PMid:17308997
Yu Z.Q., Meng Q.Y., Yuan L., Zhao Z.H., Li W., Hu X.X., Yan B.X., Fan B.L., Yu S.Y., and Li N., 2005, Comparative analysis of the pig BAC sequence involved in the regulation of myostatin gene, Science in China Series C, Life Sciences, 48(2): 168-180
http://dx.doi.org/10.1007/BF02879670 PMid:15986890
http://dx.doi.org/10.1360/03yc0217 PMid:15986890
Zhang D.C., Shao Y.Q., Su T.F., and Jiang S.G., 2007, Analysis of genomic structure and promoter characterization of mud carp (Cirhinus molitorella) β-actin gene, Journal of Fishery Sciences of China, 14(3): 345-351 (张殿昌, 邵艳卿, 苏天凤, 江世贵, 2007, 鲮β-肌动蛋白基因和启动子的克隆及序列特征分析, 中国水产科学, 14(3): 345-351)
Zimmers T.A., Davies M.V., Koniaris L.G., Haynes P., Esquela A.F., Tomkinson K.V., Mcpherrom K.A., Wolfman N.M., and Lee S.J., 2002, Induction of cachexia in mice by systemically administered myostatin, Science, 296(5572): 1486-1488
http://dx.doi.org/10.1126/science.1069525 PMid:12029139